Glosario Química / Término
Masas, espectrometría de
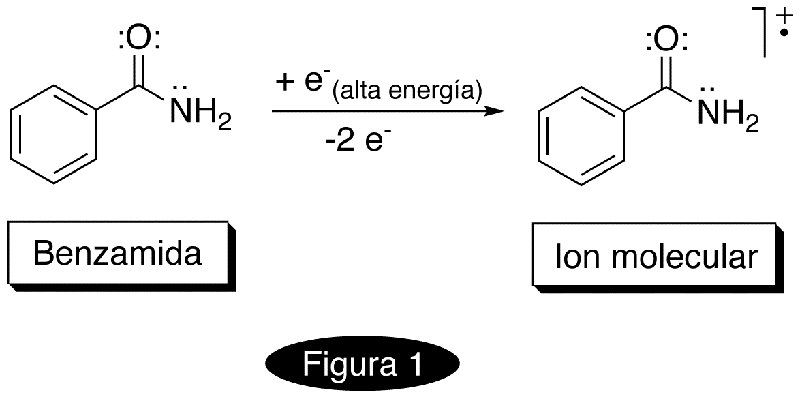
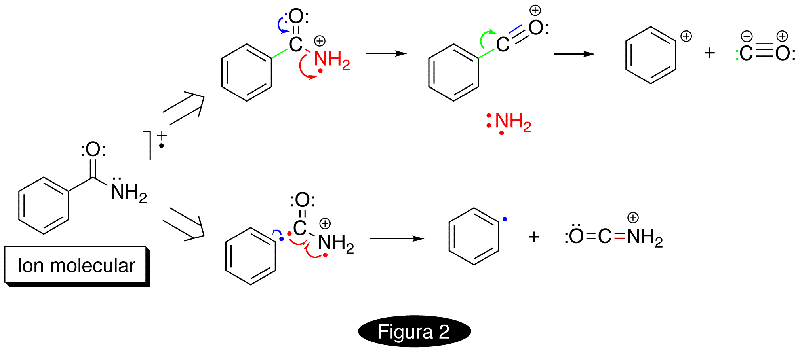
Análisis de carácter destructivo que permite determinar en una muestra detalles estructurales de sus moléculas, entre otros, su peso molecular, si en éstas se encuentran presentes ciertos grupos funcionales, si hay anillos aromáticos, si poseen una cadena alifática, si ésta se encuentra ramificada, su extensión, etc. El experimento se desarrolla en un equipo denominado espectrómetro de masas. Existen diferentes técnicas para llevar a cabo esto; entre las más empleadas se encuentra la técnica de espectrometría de masas por impacto electrónico, en la cual una muestra es vaporizada al alto vacío (hasta 10-6 mmHg, 133 µPa) y hecha reaccionar con un haz de electrones de alta energía (de unos 70 eV, equivalentes a 6.75 MJ/mol, que es la energía que poseen los fotones de un haz de rayos-X de 17.8 nm de longitud de onda) dentro de un compartimento denominado cámara de ionización, lo que origina que sus moléculas pierdan un electrón. Los iones así generados (llamados iones moleculares, M+, cuya masa coincide con el valor del peso molecular) inician de esta manera un viaje a través de un conducto en el que el alto vacío se hace aún mayor (hasta 10-8 mmHg, 1.3 µPa) atraídos por campos eléctricos y magnéticos dispuestos a una cierta distancia de la cámara de ionización, que los aceleran. Concomitantemente, los iones moleculares, una vez formados, se fragmentan dando lugar a una serie de iones de composición más simple (y por tanto, de menor masa) que también viajan. Los iones colisionan con un detector que permite registrar sus masas, y al final, el equipo de cómputo al que se encuentra acoplado el espectrómetro entrega un diagrama llamado espectro de masas, en donde se registra la relación masa/carga (vide infra) de los iones que fueron detectados por el equipo y su abundancia relativa a manera de un histograma. La fragmentación del ion molecular no es caótica, sino que sigue una serie de tendencias que han sido muy ampliamente estudiadas y que se desarrollan siguiendo una lógica química, tendiendo a formarse los iones con la mayor estabilidad posible. Al ion que se detecta en mayor proporción se le da el nombre de ion del pico base y en el espectro de masas a su línea se le asigna una abundancia relativa arbitraria del 100%; la abundancia con la que se detectan el resto de los fragmentos es reportada como una relación porcentual relativa al pico base. Ocasionalmente, como en el caso de muchos de los compuestos aromáticos, el ion molecular puede alcanza una condición de notable estabilidad, por lo que puede identificársele muy fácilmente (incluso, llega a constituirse como el pico base); en contraste, en el caso de los compuestos alifáticos el ion molecular a veces no es registrado por el equipo. La descripción de la manera en la que se fragmenta un ion molecular se conoce como patrón de fragmentación. Considérese el proceso de ionización que sufre la benzamida dentro de la cámara de ionización (Figura 1) para formar el ion molecular. El símbolo indica que el ion molecular así formado posee un electrón menos de los representados por la estructura de Lewis, aunque no se indica cuál (los iones moleculares por fuerza observan esta condición, por lo que se les define como radicales iónicos; siempre que un ion posea una condición de balance electrónico tal que permita definirlo como radical iónico, debe trazarse este símbolo acompañando a la representación de su estructura). El ion molecular de la benzamida sufre entonces las serie de degradaciones que aparecen en la Figura 2. Las especies iónicas son entonces registradas por el detector del equipo y se reportan dentro del espectro de masas de esta sustancia (Figura 3). La masa de los iones está expresada en términos de su relación masa/carga (m/z o m/e; la carga normalmente vale la unidad, dado que los iones que fundamentalmente se forman poseen solamente una carga positiva; de esta manera, su valor coincide con el de su peso fórmula). Otra técnica que se emplea es la de espectrometría de masa por ionización química, en la que la remoción del electrón de la muestra para formar el ion molecular la lleva a cabo una especie cargada de alta energía (como el CH5+, derivada del uso de metano). Una tercera opción, inidicada para las muestras que no pueden transformarse en vapor ya sea porque su punto de ebullición es muy elevado o porque se descomponen térmicamente, es la conocida como espectrometría de masas por FAB+ (de Fast Atom Bombardment, bombadeo con átomos rápidos), en donde la muestra se disuelve en un líquido viscoso (matriz) y desde allí es desabsorbida por medio de un bombardeo con átomos de xenón o argón energizados. Los iones que se producen, tanto negativos como positivos, son expulsados hacia el sitio donde se llevará a cabo la medición. Los espectrómetros de masas son muy versátiles y existen diferentes experimentos que pueden llevarse a cabo. Con los equipos con alta resolución por ejemplo es posible diferenciar iones de masas cuya variación es considerablemente pequeña; por ejemplo, en uno de tales equipos es posible diferenciar los iones cuyo valor nominal de m/z es 55: C3H3O (55.0184), C2H3N2 (m/z = 55.0297), C3H5N (55.0422) y C4H7 (55.0548). Por otro lado, es muy frecuente acoplar un equipo de masas con uno de cromatografía de gases (v.) para el análisis inmediato de mezclas (conexión tipo tándem que se conoce de manera familiar como gases-masas). Como se mencionó al principio, este ensayo es destructivo, esto es, la muestra analizada no puede recuperarse; no obstante, gracias a los importantes adelantos técnicos conseguidos, las cantidades que de muestra se requieren para realizar el análisis pueden llegar a ser mucho menores a 1 mg. En inglés: mass spectrometry. El espectro de masas de la Figura 3 se tomó del sitio de SDBSWeb: http://riodb01.ibase.aist.go.jp/sdbs/ (National Institute of Advanced Industrial Science and Technology). Acceso: febrero 16 de 2010.
Enlace permanente: Masas, espectrometría de - Fecha de creación: 2017-12-06
Novedades
Glosarios especializados
Este sitio web es posible gracias a que muestra publicidad en línea a sus visitantes.Por favor, ayude a que pueda seguir existiendo deshabilitando su bloqueador de anuncios (adblocker).
Muchas gracias.