Glosario Termodinámica / Término
Entropía
Es la magnitud física que mide la parte de la energía que no puede utilizarse para producir trabajo. Es una función de estado de carácter extensivo y su valor, en un sistema aislado, crece en el transcurso de un proceso que se dé de forma natural.
En termodinámica, la entropía (simbolizada como S) es la magnitud física que mide la parte de la energía que no puede utilizarse para producir trabajo. Es una función de estado de carácter extensivo y su valor, en un sistema aislado, crece en el transcurso de un proceso que se dé de forma natural. La entropía describe lo irreversible de los sistemas termodinámicos.
Ecuaciones
Esta idea de desorden termodinámico fue plasmada mediante una función ideada por Rudolf Clausius a partir de un proceso cíclico reversible. En todo proceso reversible la integral curvilínea de δQ/T sólo depende de los estados inicial y final, con independencia del camino seguido (δQ es la cantidad de calor absorbida en el proceso en cuestión y T es la temperatura absoluta). Por tanto ha de existir una f(x) del estado del sistema, S=f(P,V,T), denominada entropía, cuya variación en un proceso reversible entre los estados 1 y 2 es:
Téngase en cuenta que como el calor no es una función de estado se usa δQ en lugar de dQ.
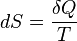
La entropía física, en su forma clásica, está definida por la ecuación:
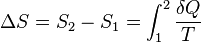
O más simplemente, cuando no se produce variación de temperatura (proceso isotérmico):
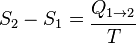
Donde S es la entropía, 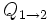 la cantidad de calor intercambiado entre el sistema y el entorno y T la temperatura absoluta en kelvin). Los números 1 y 2 se refieren a los estados iniciales y finales de un sistema termodinámico.
la cantidad de calor intercambiado entre el sistema y el entorno y T la temperatura absoluta en kelvin). Los números 1 y 2 se refieren a los estados iniciales y finales de un sistema termodinámico.
El significado de esta ecuación es el siguiente:
Cuando un sistema termodinámico pasa, en un proceso reversible e isotérmico, del estado 1 al estado 2, el cambio en su entropía es igual a la cantidad de calor intercambiado entre el sistema y el medio dividido por su temperatura absoluta.
De acuerdo con la ecuación, si el calor se transfiere al sistema, también lo hará la entropía, en la misma dirección. Cuando la temperatura es más alta, el flujo de calor que entra produce un aumento de entropía menor. Y viceversa.
Las unidades de la entropía, en el Sistema Internacional, son el J/K (o Clausius) definido como la variación de entropía que experimenta un sistema cuando absorbe el calor de 1 Jules (unidad) a la temperatura de 1 Kelvin.
Cuando el sistema evoluciona irreversiblemente, la ecuación de Clausius se convierte en una inecuación:
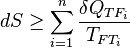
Siendo la sumatoria de las i fuentes de calor de las que recibe o transfiere calor el sistema y la temperatura de las fuentes. No obstante, sumando un término positivo al segundo miembro, podemos transformar de nuevo la expresión en una ecuación:
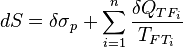
Al termino σp, siempre positivo, se le denomina producción de entropía y es nulo cuando el proceso es reversible salvo irreversibilidades fruto de transferencias de calor con fuentes externas al sistema. En el caso de darse un proceso reversible y adiabático, según la ecuación, dS=0, es decir, el valor de la Entropía es constante y además constituye un proceso isoentrópico.
Enlace permanente: Entropía - Fecha de actualización: 2019-06-24 - Fecha de creación: 2018-08-31